はじめに
日常臨床で口腔内を診察する歯科医師が口腔癌に遭遇することは、稀ではありますが、口腔の専門家として早期発見に貢献することが望まれます。口腔癌の早期発見のスキルは後述することとして、ここでは歯科医師として最低限知っておきたい近年の遺伝子レベルで捉えた口腔癌の生物学的特性の概要を簡単に述べてゆきます。癌は細胞内の遺伝子変異に起因する遺伝子の病気と言われ、口腔癌も同様に遺伝子の病気であることに変わりはありません。近年の癌研究の進歩によって発癌に関与する多くの遺伝子が単離・同定され、癌の発生、悪性化の機構が遺伝子変化との対応で捉えられるようになってきました。
発生要因
口腔癌の発生原因には遺伝的要因と環境要因の二つが重要です。
遺伝的要因
癌は人間の体のどこかの細胞に遺伝的変異が起こって出現する突然変異細胞が生体の防御機構から逃れて増殖を続ける結果、様々な組織の機能を障害し、個体を死に至らしめる疾患です。細胞内で変異を起こし、癌化に関連している遺伝子を大きく癌遺伝子と癌抑制遺伝子と分類します。口腔癌では癌遺伝子の活性化と癌抑制遺伝子の不活性化(図1)といった遺伝的要因で癌化が生じます。これらの遺伝子は細胞増殖、分化、細胞死に関連しており、無限増殖、分化の停止(未分化)、細胞死の回避が生じます。これらは、癌の基本的な生物学的特徴です
環境要因
環境中の発癌物質に曝されることによる遺伝子変異です。口腔癌で関連がわかっている環境要因での危険因子は喫煙、アルコール摂取、ヒトパピローマウイルス(HPV)です。 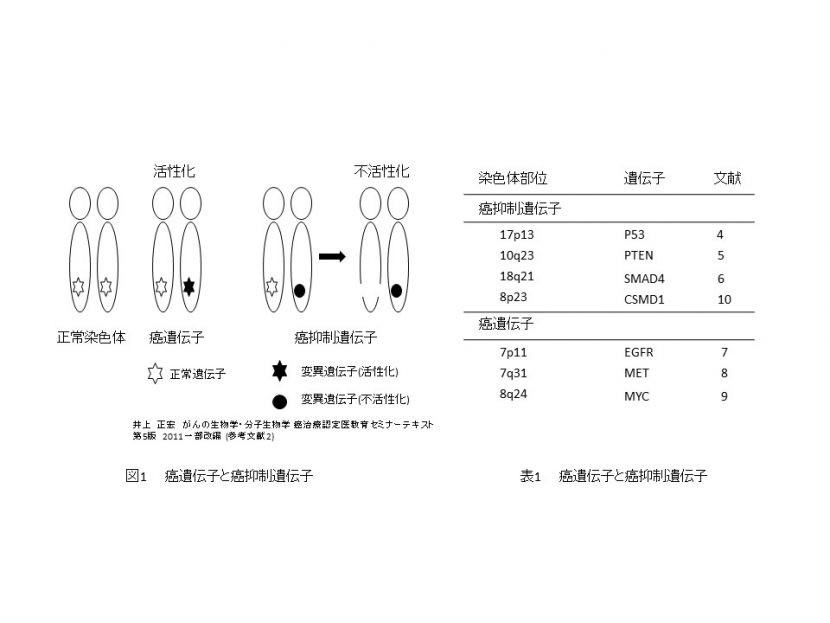
癌遺伝子の活性化と癌抑制遺伝子の不活性化
癌遺伝子は正常細胞に内在し、正常細胞の機能にも重要な働きをしています。相同遺伝子のどちらかに遺伝子機能を活性化させるような変異(点突然変異、遺伝子増幅、染色体転座など)が起これば機能を得ます。癌抑制遺伝子の不活性化にとは相同遺伝子の双方が不活性化することで癌抑制機能を失い癌化が促進します。口腔癌で明らかに関連性が知られている代表的な遺伝子は表1の如くです。
無限増殖性
口腔癌の無限増殖性は細胞周期を制御する癌抑制遺伝子p53とretinoblastoma(RB)経路の破綻によるものと考えられています。細胞周期はG1期、S期(DNA合成期)、G2期、M期(分裂期)からなる細胞周期を繰り返して増殖します。G1期からS期に移行、G2期からM期に移行する際に細胞が正しく細胞周期を進行させているかどうかを監視し、異常が有る場合に進行を停止、減速するチェックポイントがそれぞれ存在し癌細胞では特にG1/Sチェックポイントの制御異常がしばしば認められます。RBはG1/Sチェックポイントの鍵分子であり、不活性化によって細胞周期の制御が不能になります。p53もG1/Sチェックポイントを負に制御しているが、不活性化によって細胞増殖の「ブレーキ」が効かない状態となります。
ヒトパピローマウイルス(HPV)
HPVタイプ16,18のE6/E7遺伝子はウイルス性発癌タンパクをコードしてp53、RBタンパクと結合し、癌抑制遺伝子の機能を不活性化することが明らかになっています。
不均一性
口腔癌は正常細胞の染色体に変異が入って異常増殖した均一ながん細胞の集団ではなく不均一な細胞の集団です。少なくとも二つのサブクラス(亜綱分類)、HPV陽性(約20%)、HPV陰性(約80%)腫瘍に分類されます。HPV陽性腫瘍は60歳以下で近年頻度は増加しており予後は比較的良好とされています。HPV陰性腫瘍の内、約65%はp53遺伝子変異を始めとしたたくさんの遺伝子変化があり予後は悪いとされています。
II 発生経路
口腔癌の発生由来上皮は上部消化管裏層粘膜である扁平上皮です。口腔癌の発生進展にはこの正常扁平上皮細胞に上記発生要因が加わり、口腔前癌病変(白板症)となります。口腔前癌病変中の細胞に新たな遺伝子変異が蓄積し悪性の原発腫瘍として進展してゆきます。このように段階的に細胞中に変異が蓄積して病態が悪性化してゆくことを多段階発癌(図2)といいます。
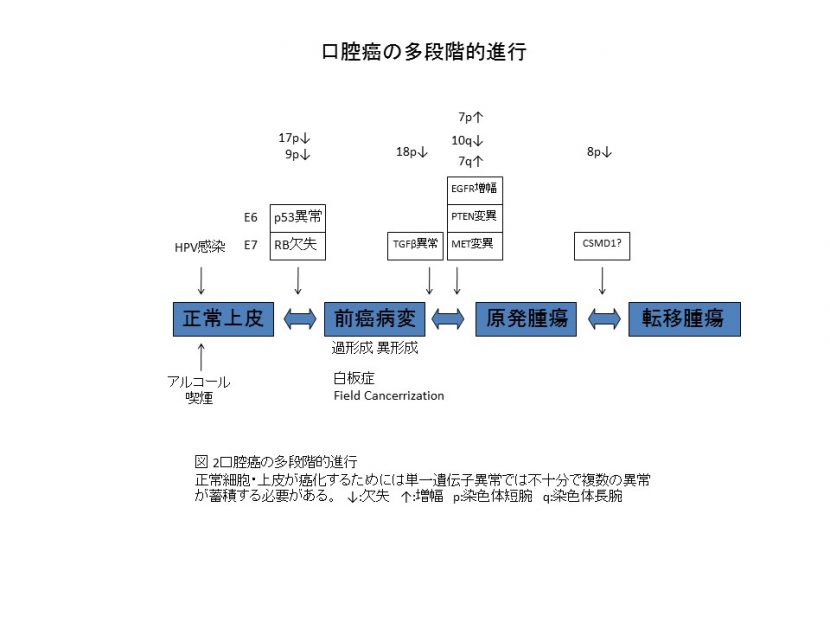
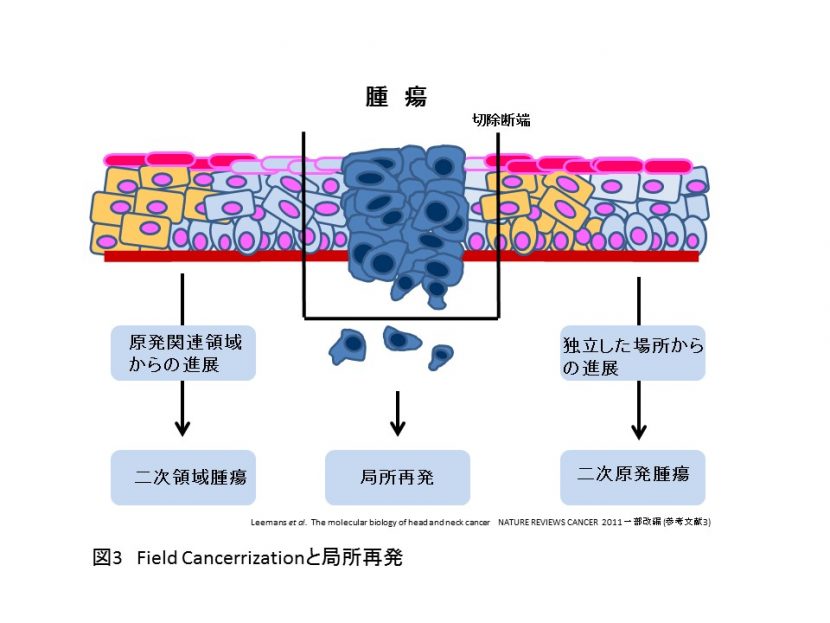
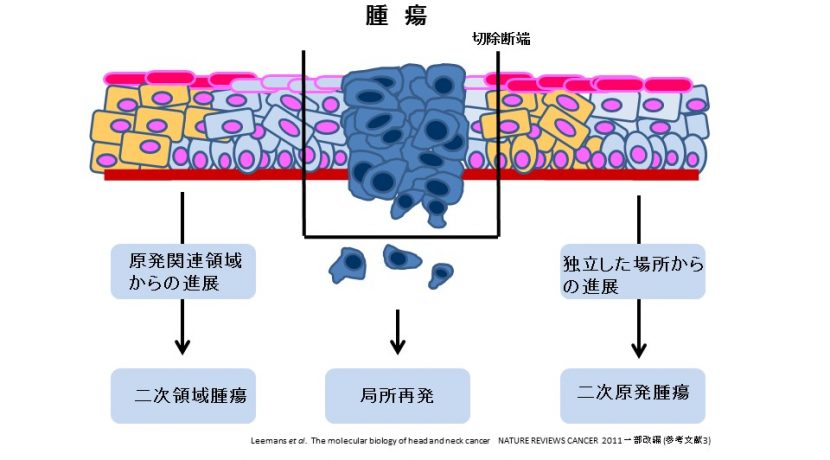
また、口腔癌では口腔前癌病変の病理学的特徴とされる異形上皮が多発し、独立した場所から癌が多発する(Field Cancerrization 図3)ことが知られています。原発腫瘍に近接した部位や離れた部位に存在する病理組織学的に正常と考えられる粘膜にすでにp53遺伝子変異が生じており、発癌過程の初期段階が始まっているためと考えられています。
発癌過程の後期段階では増殖シグナルの獲得が重要です。細胞は外部からの刺激に適切に応答して細胞分裂していますが、癌では分裂シグナルが過剰になっています。口腔癌で関連性が知られている代表的増殖経路は上皮成長因子受容体(EGFR)シグナル伝達経路で、EGFがEGFRと結合することによって、受容体が活性化され、さらに細胞内シグナル分子MAPK経路、PI3K-Akt経路が活性化します。他にも細胞増殖を負に制御しているトランスフォーミング増殖因子(TGFβ)シグナル伝達経路の不応化、耐性機序に関連したMET遺伝子増幅が存在します。
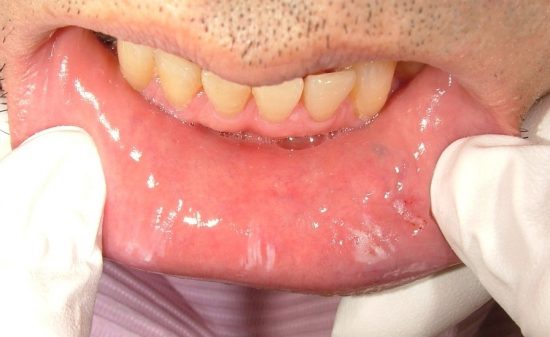
白板症
1978年WHOの診断基準によれば「口腔粘膜に生じた摩擦によって除去出来ない白色の板状あるいは斑状の角化性病変で、臨床的あるいは病理組織学的に他のいかなる疾患にも分類されないような白班」と定義されています。代表的な前癌病変で染色体9p欠失などにより正常粘膜上皮が過形成を起こします。ついで17p欠失などによりp53異常を生じ上皮異形成が生じる。この過形成・異形成といった病理学的特徴を持った状態を前癌病変と呼びます。
Field Cancerrization(広域発癌)
1953年、Slaughterらによって提唱された概念で、発癌物質に暴露された粘膜は、広い範囲(Field)にわたって「条件づけられた上皮」の場、あるいは「運命づけられた粘膜」が存在し、さらに発癌物質に曝されることにより前癌病変とされる異型上皮が多発し扁平上皮癌が多発するという仮説です(図2)。
増殖経路
・上皮成長因子受容体(EGFR)シグナル伝達経路
上皮成長因子(EGF)は細胞の増殖や成長を制御する成長因子で、細胞膜を貫通して存在する受容体が上皮成長因子受容体(EGFR)です。EGFがEGFRに結合、リン酸化されると、MAPK経路、JAK-STAT経路、PI3K-AKT経路などの細胞内経路が活性化して核内にシグナルを伝達します。口腔癌の中には、EGFRシグナル伝達経路において体細胞変化によりEGF刺激に依存せず、シグナルが自己活性化しているものがあります。
・トランスフォーミング増殖因子(TGFβ)
正常上皮細胞の増殖はトランスフォーミング増殖因子(TGFβ)により阻止されるが、口腔癌の中にはTGFβの増殖抑制作用から体細胞突然変異や関連する鍵遺伝子の染色体欠失によって反応性が失われたものがあります。
・PI3K-PTEN-Akt経路
Phosphoinositide 3-kinase(PI3K)はイノシトールリン脂質のリン酸化を行う酵素である。イノシトールリン脂質は真核生物の細胞膜を構成する成分の一つであり、PI3Kをはじめとしたキナーゼ(リン酸化酵素)の触媒作用を受けてプロテインキナーゼB(PKB)/Aktを活性化を起こします。このシグナル伝達経路はPI3K-Akt経路と呼ばれるが、細胞死の回避に関連しています。口腔癌における体細胞変異、遺伝子変化とは、このPI3K-PTEN-Akt経路の活性化であることが多いと言われています。
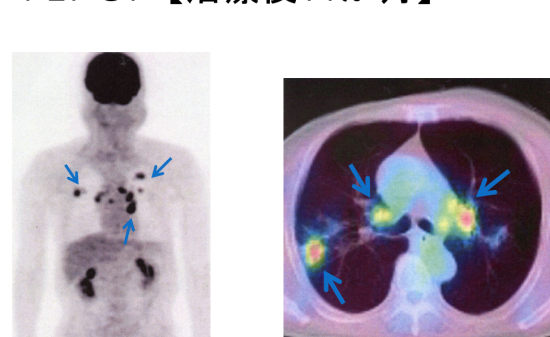
転移
口腔癌の転移播種は頸部リンパ節である。転移予知が可能な原因遺伝子は同定されていない。染色体短腕8上の癌抑制遺伝子CSMD1遺伝子の関与が示唆されています。
おわりに
孫子の兵法「彼を知り己を知れば百戦にして殆うからず」は、口腔癌といった厄介な病に相対するわれわれ臨床家に大きな示唆を与えます。発癌のメカニズムを知ることは敵をよく知るということです。まだまだ解明されていないことだらけですが、現在までに明らかになった口腔癌に関する分子生物学的知見の一端を述べてきました。これらの知見を頭の片隅に思い浮かべながら口腔の専門家として早期発見に貢献していただけたら幸いです。
参考文献
- 日本がん治療認定医機構教育委員会 癌治療認定医教育セミナーテキスト第5版 2011
- C.Rene Leemans et al. The molecular biology of head and neck cancer. Nature REVIEWS CANCER. Vol.11 No.1, 9-22 2011
- Opitz,O.G. et al. CyclinD1 overexpression and p53 inactivation immortalize primary oral keratinocytes by a telomerase-independent mechanisum. J.Clin. Invest. 108,725-732 2001
- Okami,k. et al. Analysis of PTEN/MMAC1 alterations in aerodigestive tract tumors. Cancer Res. 58, 509-511 1998
- Bornstein,S et al. Smad4 loss in mice causes spontaneous head and neck cancer with increased genomic instability and inflammation. J.Clin.Invest. 119,3408-3419 2009
- Sheu et al. Functional genomic analysis identified epidermal growth factor receptor activation as the most common genetic event in oral squamous cell carcinoma. Cancer Res. 69, 2568-2576 2009.
- Seiwert,T.Y. et al. The MET receptor tyrosine kinase is a potential novel therapeutic target for head and neck squamous cell carcinoma. Cancer Res. 69, 3021-3031 2009
- Goessel,G. et al. Creating oral squamous cancer cells:a cellular model of oral-esophageal carcinogenesis. Proc.Natl Acad.Sci.USA 102,15599-15604 2005
- Sun,P.C. et al. Transcript map of the 8p23 putative tumor suppressor region. Genomics 75,17-25 2001










 PAGE TOP
PAGE TOP