ナノテクノロジーと歯科医療
はじめに
ナノサイエンス/ナノテクノロジーはナノメーター(10-9m)スケールの物質を扱うサイエンス/テクノロジーである。1 nm はほぼ DNA のサイズであり、10μm スケールの細胞よりはるかに小さい領域、特に 1-100 nm の大きさを対象とする。このサイズの物質を操作、加工したり、観察したりする技術の進歩とともに、フラーレンやカーボンナノチューブ等の新しい材料の発見もあり、様々な施設で研究が盛んに行われている。ナノ医療とは、ナノテクノロジーを医療に応用するものである。ナノマシンと呼ばれるナノサイズの一種のロボットを用いて病気を治療しようという計画もあるが、現在集中的に研究され、一部は既に実用化されているものは、主にナノスケールの微粒子やデバイスを用いた新しい診断・治療法である。以下に、ナノテクノロジーの実際の使用例について述べる。
ナノテクノロジーとドラッグデリバリーシステム(DDS)
一般に、経口剤でも注射剤でも薬剤を血流に介して運ぶ場合、ヒト毛細血管の直径は約5ミクロン(1ミクロンは1/1000ミリメートル)なので、薬のサイズはそれ以下の1ミクロンか、あるいはずっと小さい数ナノメートル(nm)(1ナノメートルは1/1000ミクロン)にすることが求められる。
実際、DDSとして利用される微粒子のサイズは、150nm程度のものが現在中心を占めている。たとえば、がん、再生医療などを対象にしたDDSについては、薬物を封入するリポソームや高分子ミセルのサイズは数100nmの範囲にある微粒子製剤である。この微粒子のサイズはDDS製剤にとってはとても重要である。なぜならば、微粒子のサイズが数nm以下と小さい場合、一般にヒト腎臓から尿中に容易に排泄されてしまうため体内に滞留させることが出来ずに薬剤としての効き目を発揮することが出来ない。一方、微粒子のサイズが大きすぎても不都合で、400nm以上になると今度は免疫機構が働き、マクロファージなどによる異物排除により体内から素早く排除されてしまうため、これもまた薬剤としての効き目を発揮することが出来ない。それゆえにDDS製剤としては上述した微粒子のサイズが必要である。そこで薬剤を血液に介して運ぶ場合には「ナノテクノロジー」(10億分の1メートルスケールの領域での製造技術)によって薬剤を膜で包み込み、病変部に到達させ、そこで薬剤をリリースして治療効果を高める手法が取られている。以下に、癌組織の血管の漏出性を利用し、この微粒子を癌に集積させる概念について説明する。
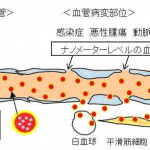
癌組織や炎症部位の血管内皮細胞間には正常な血液内皮細胞細胞とは異なり200nm程度の広い隙間が開口しており、100nm程度にサイズが制御された微粒子製剤や高分子製剤を癌
組織に集積させることが可能なことを明らかにしている(図1)。つまり、抗癌剤をナノ粒子に封入できれば、正常な血管壁からは漏れ出すことなくがん組織だけに入り、病変部位の薬剤濃度だけが上昇する。更に、癌組織はリンパ管が未発達で薬物の回収機構が不完全なため結果的に薬剤が、癌組織に長時間滞留・残存することになる。このように抗癌剤をナノテクノロジーによりナノ粒子にすることでDDS製剤としての機能、すなわち、医薬品を必要な場所に、必要な時間、必要な量だけ送達することが即発揮できることから、この原理を利用した抗癌剤の開発が活発に行われており、いくつかのDDS化された抗癌剤が実用化されている。
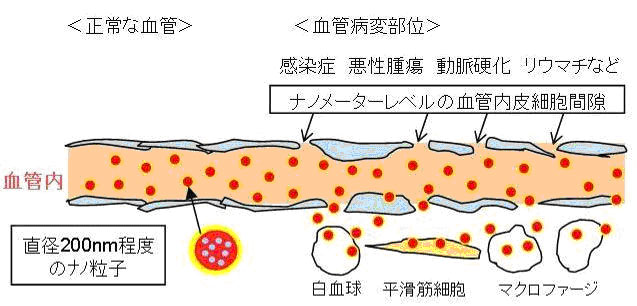
図1ナノスケール微粒子加工による生体適合性
ナノスケール微粒子を表面に結合させ応用されているものとして医療用のカテーテルがある。カテーテルは、体外から体腔内に薬剤などを注入したり、体腔にたまった液体を体外に取り出すために使われる内径2~3.5mmの細いチューブである。カテーテルは、シリコーンなど弾力性の高い高分子材料が基盤材料として作られているが、長期間にわたって使用する場合、患者の体との接着部分からの細菌感染と、それに伴う病態悪化の懸念が大きな問題となっている。それは、生体とカテーテル材料との親和性が乏しいため、組織とカテーテルの隙間が細菌の侵入経路になるためと言われている。
そこで、カテーテルの基盤材料であるセラミックスの「硬い・もろい」という欠点を克服するために、生体適合性が良いと考えられているナノテクノロジーを用いたナノ微粒子をカテーテルの表面に結合させることが考案された。例として、ソフセラ社が開発した「焼成ハイドロキシアパタイト高分子分散性ナノ粒子」(SHAp)が挙げられる(図2)。SHApをカテーテル表面に結合させたソフトセラミックスを皮膚直下に留置することにより、細菌侵入を防止する。つまり、SHApは細胞接着の乏しい材料(例えば、シリコーンやポリ乳酸など)と皮膚や皮下組織細胞との接着性を向上させ、それらの細胞との高い接着強度を与えることになる(図3)。また、カテーテルなどの医療の分野のみならず、様々な産業への応用が試みられている。

ナノテクノロジーを用いた組織再生
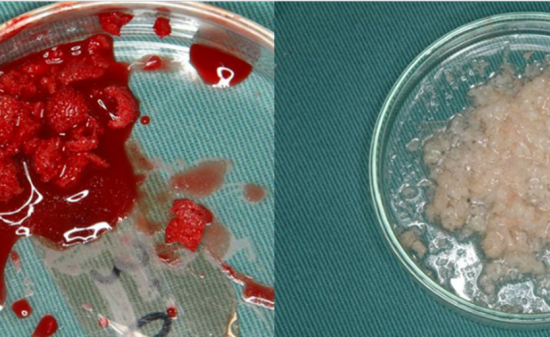
バイオナノテクノロジーで注目される分野の1つに再生医療があり、培養技術が期待されている。しかし細胞を規則的かつ煩雑な構造を構築して、器官を形成し、さらに維持するためには細胞の生存に適した環境下で酸素や栄養を供給しなければならない。現在はまだ臓器ユニット培養にはいたっておらず、培養を目的とした細胞配置に適した微細構造体を必要とされている。そこで近年、細胞シートという新しい概念が開発された(図4)。なぜシート状で作成するのかというと、 人間の体の組織や臓器はシート状の細胞からできている構造が基本であり、いろいろな形状に折り重なって血管や臓器などの立体的な組織ができているためである。 現在では、温度により変化するナノ薄膜上で細胞シートを作成することにより、皮膚や角膜、歯根膜や心臓の筋肉などの細胞シートを作ることができる。この培養表面上に作られた温度応答性ナノ薄膜にナノテクノロジーが活かされている。この薄膜状に培養した細胞は従来のような酵素を使わずに培養温度を変えるだけで剥がすことができるようになる。培養細胞は酵素処理を受けないので、細胞と細胞との間に存在する接着性タンパク質が破壊されず、培養細胞は一枚のシートとして得られる。また、培養中に細胞とナノ薄膜との間に形成された接着性タンパク質も保持されるため、細胞シートは生体組織へ速やかに生着し、細胞シート同志を積層化させることもできる。したがって、細胞シートは片面が糊なる接着たんぱく質を有しているため、移植部に直接貼って体と一体化でき、角膜上皮移植では、 数分程度で接着できるため手術時間の大幅な短縮が可能となる。しかも、その細胞シートは酵素処理によって細胞本来の機能も失われることなく保持される。また、 性質の違う細胞シートを組み合わせて肝臓や腎臓といった複雑な組織を再生することも可能になりつつある。また、もう一つのメリットとしては、細胞シートは患者本人の細胞から培養できるため、拒否反応もなくドナー不足に悩まされることもない。
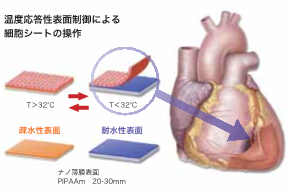
図4細胞シートの作成および応用例
温度応答性のナノ薄膜表面を用いることにより、培養後 32°Cまで温度を下げるとナノ薄膜表面は親水性になって、細胞をシートのままきれいに剥がすことができる。
ナノテクノロジーの歯科医療への応用
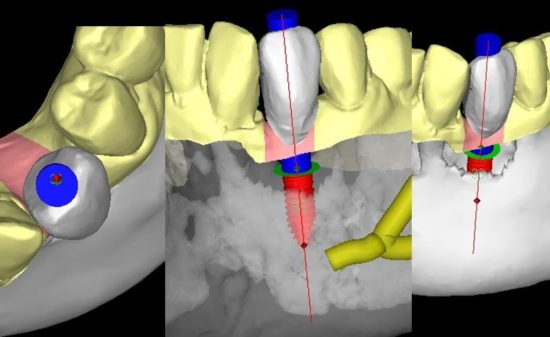
デンタルインプラント治療と軟組織再生
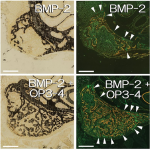
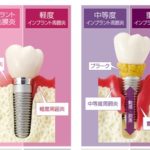
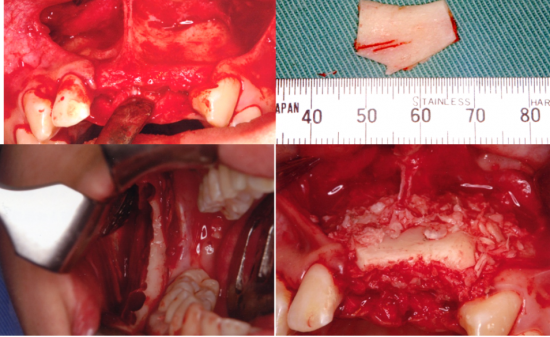
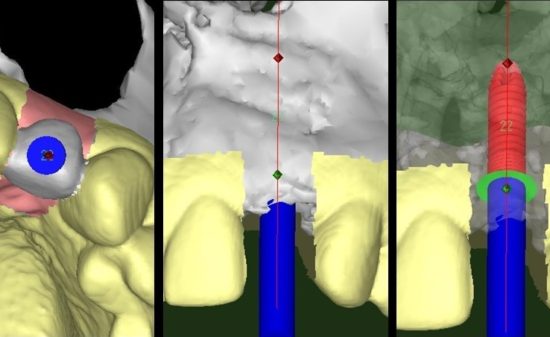
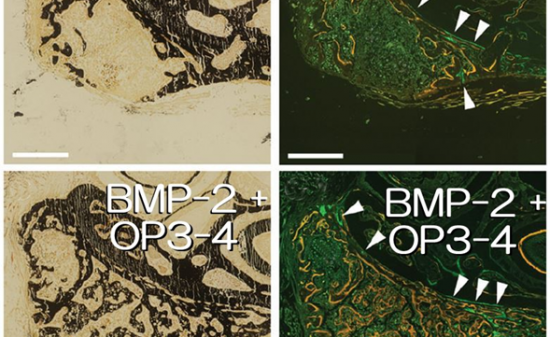
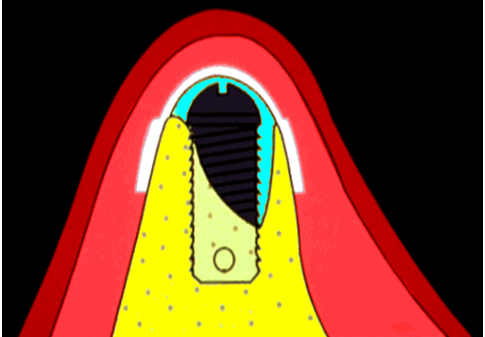
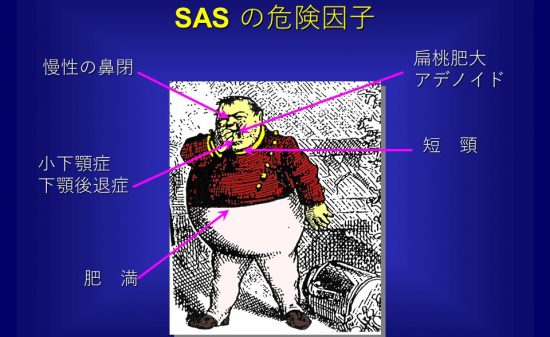
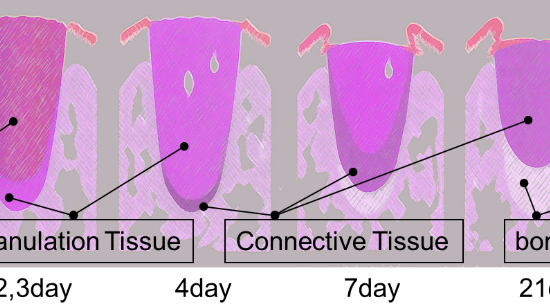
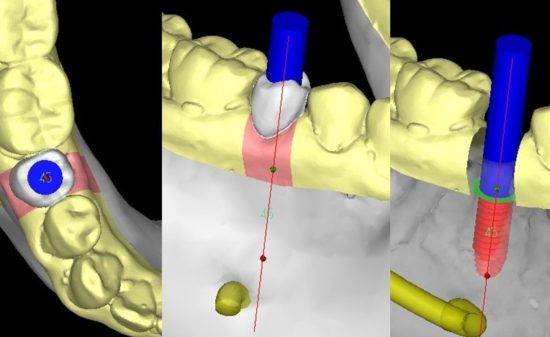
近年、インプラント治療の需要が高まり、様々な口腔内環境の患者に対してのインプラント治療が行われている。その中には、付着歯肉の幅が少ないため、インプラント埋入のみでは著しい審美障害やインプラント周囲炎を引き起こす可能性が高い症例に遭遇することがある。現在このような患者に対して、結合組織移植による軟組織の増生が行われている。しかし、移植する結合組織は主に口蓋部からであり、インプラント埋入した部位と別の部位から結合組織を採取しなければならず、手術時間の延長および患者の身体的負担を強いる事になる。そこで、今回我々は、ソフセラ社が製造しているSHApに着目し、このナノ粒子が軟組織造成の必要性がある患者のインプラント治療やその他の歯科治療に応用できないかを検討している。このSHApはコラーゲン線維を誘導すると言われており(図4)、その後貪食細胞により吸収されることが動物実験レベルで証明されている(図5)。したがって、軟組織が不足しているインプラントの歯槽骨の骨膜上に移植する事により結合組織を再生させ、その後SHApが吸収されることが予想される。したがって、移植したSHApが残存せずにコラーゲン組織に置換されることになる。このことは、インプラント周囲の軟組織再生に使用される移植剤としては今までにない画期的な移植剤として考えられ、現在、動物実験レベルで検討中である。
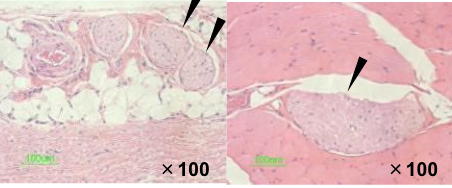
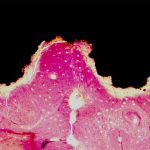
図5マウスの背部皮下にSHApを注射し、1週間後の組織像を示す。SHAp周囲にコラーゲン線維の形成が認められた。矢印はコラーゲン線維を示す。
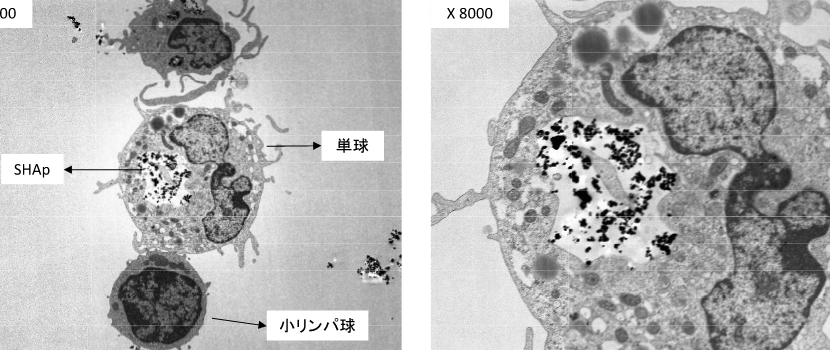
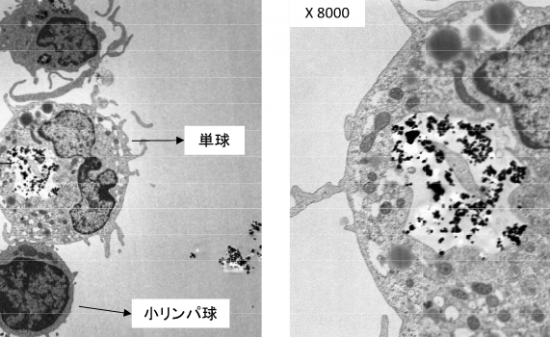
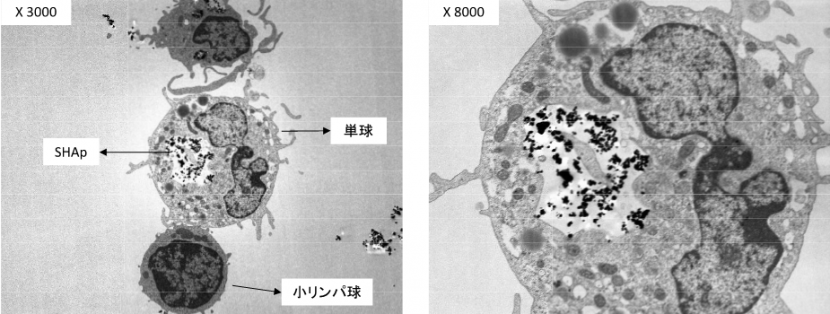 図6 SHApが単球細胞により、貪食される時のSEM像
図6 SHApが単球細胞により、貪食される時のSEM像
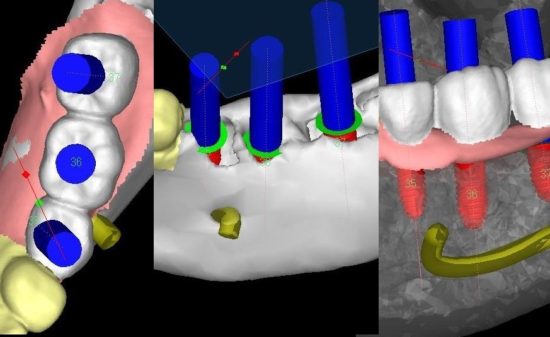
デンタルインプラント治療と硬組織再生
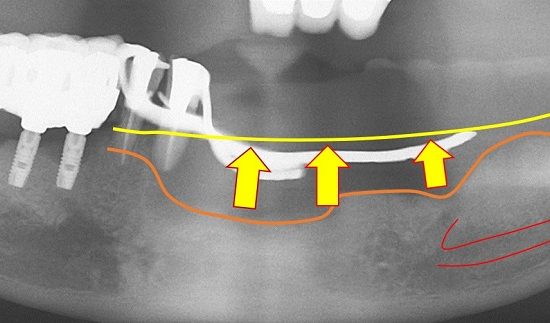
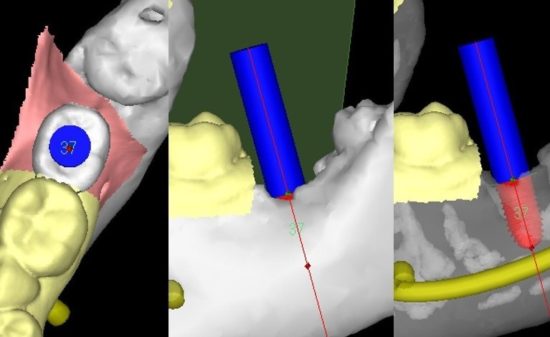
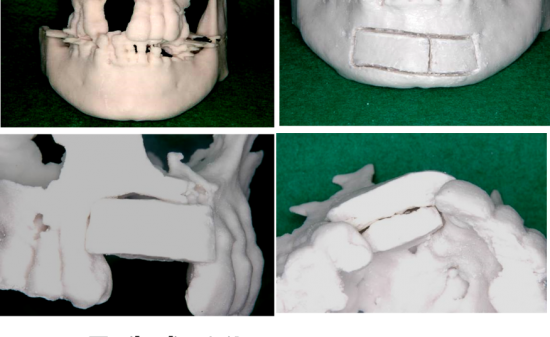
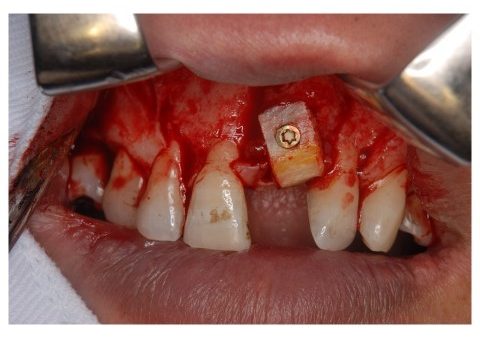
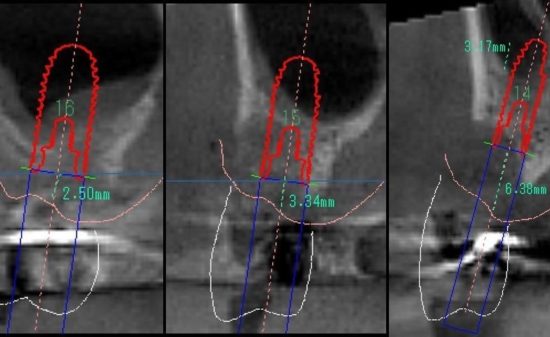
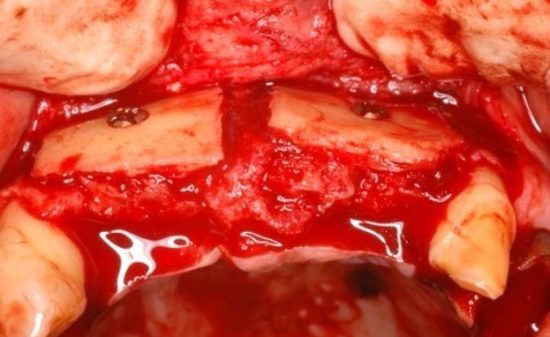
歯槽骨量が不足し、骨移植なしではインプラント埋入が不可能な症例に遭遇する場合があ
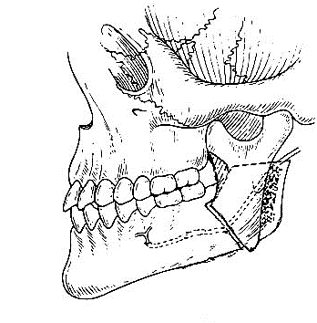
る。このような患者に対して一般的に、オトガイ部や下顎枝部より骨採取し、GBRやベニアグ
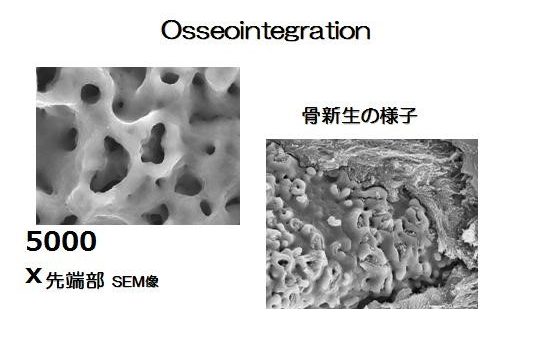
ラフトにより骨造成が行われている。しかし、手術侵襲が高く、症例によっては多量の骨が必要な場合があり、片側のみでは採骨量が不足することもある。したがって、自家骨ではなく骨補填剤のみで骨造成を行えれば、低侵襲でかつ安全なインプラント治療を行う事が出来ると考えられる。しかし、移植した骨補填剤が吸収されず残存したり逆に、吸収速度が早すぎても、それに骨形成が追いついて行かず、骨形成が予想した様に行われない場合がある。また、移植した骨補填剤が生体内で異物として感知され、感染を引き起こしてしまうこともある。そのため、骨補填剤に求められる用件として吸収と骨形成が同じような速度でかつ、感染に強いものでなければならない。そこで、軟組織造成と同様にソフセラ社製のSHApに着目した。ハイドロキシアパタイトは歯の主要な無機成分でありタンパク質などの吸着性、骨結合性、細胞接着性などの特性を有している。さらには、前項で示したように貪食細胞により吸収される事が示されている。また、ハイドロキシアパタイトをナノ加工することにより感染に強いSHApとなる。しかし、このSHApを用いた骨組織造成については、未だ検討されておらず、今後の研究結果によっては、すばらしい特性を有した骨補填剤となるのではないかと考えられる。
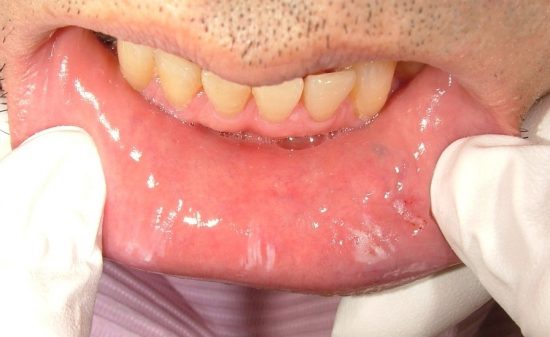
感染に強いメンブレンへの応用
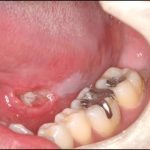
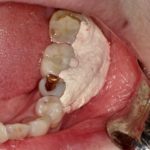
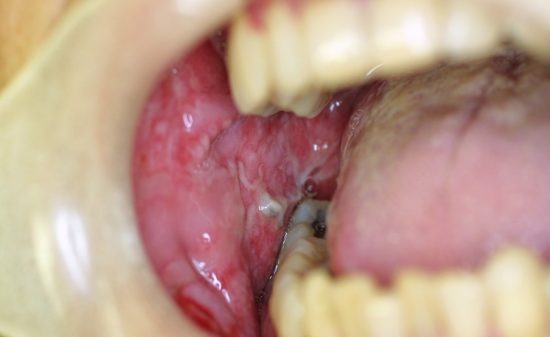
インプラント治療に対して骨造成を行うために、GBRやベニアグラフが行われている。このとき、用いられるのがメンブレンである。このメンブレンは、骨形成が行われる空間の確保および周囲組織からの組織侵入を防ぐ目的で、移植された骨を包む様に使用されている。しかし、術後メンブレンの露出による、移植骨の感染で移植した骨を除去しなければならないことがあるが、メンブレンが露出しても早期に粘膜で被覆されれば移植骨の感染を防ぐことができる。したがって、メンブレンが露出しても間もなく、粘膜が露出したメンブレン上を覆ってしまうような表面加工を考えなければならない。そこで、我々はソフセラ社のSHApに着目した。前述したカテーテルへのSHApの複合化と同様に、メンブレンの表面にSHApを複合化させることにより抗菌性を持たせ、露出してしまったメンブレン上に線維芽細胞を呼び込み、露出したメンブレン部を粘膜で早期に自然閉鎖できるのではないかと考えている。しかし、未だ研究段階であり、今後の進展が期待される。











 PAGE TOP
PAGE TOP